疾病诊断
别纠结了!这几类人,需要做移植......
谈到移植,很多患者想到的是副作用会不会特别大,会不会特别难受;第二个想到费用特别高;第三个觉得风险特别严重。医生经常说疾病想要根 治需要移植,长期缓解需要移植。大家在这个问题上反复摇摆,到底需不需要做移植?我们首先要对造血干细胞移植的治疗手段有一个清楚的认识,这样才能做出比较好的判断。
造血干细胞移植可以治疗淋巴瘤吗?
淋巴瘤是属于对放疗和化疗非常敏感的肿瘤,放疗和化疗的剂量与杀瘤效果成正相关。儿童淋巴瘤的化疗效果之所以比成人好,就是因为儿童能够耐受比成年人大得多的化疗剂量。但在成人如果把剂量提得非常高,肿瘤是清除了,但是患者的造血系统和免疫系统也遭受了不可恢复的重创。为了解决这个问题,让放疗和化疗发挥最大的效果,同时又保护机体,就可以通过骨髓移植的办法,让患者在造血干细胞的支持下,接受比较大剂量的放化疗,清扫体内所有的肿瘤细胞。另外一个原因,我们的免疫系统和血液系统都来源于造血干细胞,移植之后不仅重建了血液系统,也重建了免疫系统。未来这套新的免疫系统就能够帮助我们压住体内的肿瘤细胞,不再复发,达到长期治愈的目标。所以,造血干细胞移植一直是淋巴瘤治疗的一个非常重要的手段。正是因为如此,2018版造血干细胞移植治疗淋巴瘤中国专家共识也提到,尽管目前多种新药和新技术手段的应用提高了恶性淋巴瘤的近期疗效和长期生存,但造血干细胞移植在恶性淋巴瘤的整体治疗中仍然具有非常重要的地位。
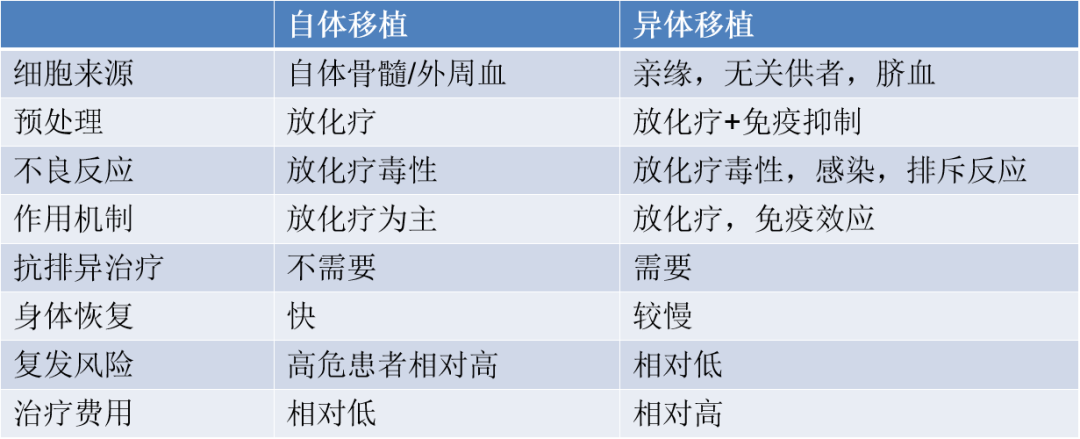
自体移植VS异体移植
造血干细胞移植可以分成两大类,一类是自体移植,即造血干细胞是来源于自己,在接受大剂量放化疗之前,先把骨髓里面的造血干细胞转移出来,体外冻存保护,再给患者大剂量的放疗化疗,清除体内常规化疗可能清除不到的残留肿瘤。这个时候骨髓也受到了一定程度的损伤,我们再把之前转移出去的那些干细胞重新回输回去,重建造血和免疫系统,这个过程叫自体干细胞移植。如果干细胞不是来源于自己的,而是来源于他人,就叫异体移植。
移植的选择——自体移植
对移植有了一定的了解之后,现在来看患者常常问到的两个问题,第一个问题,我的淋巴瘤到底需不需要做移植?第二个问题,如果需要做移植,以我目前的身体条件,到底适不适合移植?是适合自体移植还是异体移植?解答上面两个问题首先患者需要对自己的疾病有充分的认识,清晰自己淋巴瘤的亚型。
首次治疗一旦缓解“应该”做自体移植的淋巴瘤亚型:
65岁以下的套细胞淋巴瘤
绝大部分的侵袭性T细胞淋巴瘤
年轻的高危的弥漫大B细胞淋巴瘤
没有移植禁忌的多发性骨髓瘤
首次治疗一旦缓解“最 好”做自体移植的淋巴瘤亚型:
化疗敏感的淋巴母细胞淋巴瘤
双打击或双表达高级别B细胞淋巴瘤
惰性淋巴瘤转化的高侵袭性淋巴瘤
原发中枢神经系统淋巴瘤
适合作为复发后标准治疗选择的淋巴瘤:
挽救治疗敏感的复发或原发难治的弥漫大B淋巴瘤
挽救治疗敏感的第1或第2次复发的滤泡性淋巴淋巴瘤
挽救治疗敏感的复发或原发难治的霍奇金淋巴瘤
适合挽救性巩固治疗的合适选择:
复发且挽救治疗敏感、不适合异基因移植的套细胞淋巴瘤
挽救治疗敏感、不适合异基因移植的外周T细胞淋巴瘤
多次复发的某些惰性淋巴瘤
一线治疗获得部分缓解或挽救治疗敏感的伯基特淋巴瘤
移植的选择——异体移植
相较于自体移植,异基因移植的难度比较大,又有排异,时间比较长,费用也比较贵,所以异基因的选择我们要更慎重一些。
需要进行异基因造血干细胞移植的类型我们归类如下:
多次复发、原发耐药和自体移植后复发的淋巴瘤
17p缺失或TP53基因异常突变,氟达拉滨或联合免疫化疗治疗失败的慢性淋巴细胞白血病
某些高度侵袭性淋巴瘤若治疗有效,应尽早于第1次完全缓解期异基因移植,包括高危淋巴母细胞淋巴瘤(LBL)、肝脾T细胞淋巴瘤、肠病相关性T细胞淋巴瘤Ⅱ型、侵袭性NK细胞白血病。
移植需要的身体条件
什么情况适合移植?移植需要的身体条件都有哪些?第一个就是年龄,自体移植目前来讲,年龄≤75岁、一般状况良好而无明显脏器功能和合并症的老年患者,可以耐受自体移植。目前清髓异基因移植通常用于年龄≤55岁的年轻患者,非清髓异基因移植可以做到65-70岁筛选后的患者。第二个是体力状态,移植的时候会有一个身体状况评分。一般来讲,如果能够达到60分,是可以耐受自体移植的;如果能达到70分,可以耐受减低预处理毒性的异基因移植;达到80分以上可以耐受异体的清髓移植。当然了,仅仅根据日常生活状态就决定是否能做移植是远远不够的,还需要进行脏器功能的医学评估,比如评估有无冠心病、糖尿病、肝脏功能、肾脏功能等等,然后再结合患者的年龄确定是否适合所选择的移植。
淋巴瘤的精准移植
我们经常说靶向治疗、免疫治疗,移植技术和这些精准治疗技术并没有互相排斥,我们要充分的学习认识新技术、新手段,不断提高自己的认识,把这种精准治疗的概念引入到移植上。
首先,恰当的移植时机。每个患者的移植时机都是不一样的,不是“一刀切”的。我们准备移植的病人,一定要跟治疗医师进行充分的沟通,选择个体化最 佳的移植时机。
第二,要精准优化个体化的预处理方案,了解移植前疾病的临床特征、分子生物学特征、患者器官功能和免疫功能的个体化评价,都是个体化的客观指标。
第三,移植方案与新技术的结合。自体移植与CAR-T细胞技术结合,这是将来的方向。CAR-T治疗也是北京高博博仁医院正在探索和开展的研究,紧跟国际研究最 新进展。其次是靶向药与预处理治疗及移植后维持治疗的结合,可以作为协助移植起效,或者移植后控制病情的方法。
再有就是肿瘤易感基因检测与供者筛选要结合起来,比如小孩有遗传缺陷,我们要选择最 优的供者。这是北京高博博仁医院实施的新技术和移植的结合,相信我们的移植会越来越安全有效,也会让病人获得更好的治愈的效果。
作者简介

主任医师,医学博士,高博医疗(血液病)北京研究中心北京高博博仁医院血液四科(成人淋巴瘤科)主任。内科毕业于华西医科大学,2012年获得北京大学医学部内科血液病专业博士学位。2005年至2019年就职于北京大学第三医院,2019年至今就职于北京高博博仁医院。目前从事血液恶性肿瘤的多学科综合治疗,擅长淋巴瘤、多发性骨髓瘤、白血病的早期诊断,以内科化疗为主的综合规范化治疗、分子靶向治疗、自体/异体造血干细胞移植及生物治疗,对生物标志物指导下的免疫治疗有深入研究,熟悉掌握淋巴瘤的最新国际诊疗规范。参与20余项国际、国内多中心临床研究,及时掌握国际淋巴瘤、多发性骨髓瘤诊治前沿新动向。第一作者及通信作者发表中英文论文30 余篇,参编参译著作5本。
学术任职:中国老年学学会老年肿瘤专业委员会委员,中国健康管理协会健康科普专业委员会委员,中国医药教育协会造血干细胞移植及细胞治疗专业委员会委员,北京肿瘤协会临床研究专业委员会委员,北京市医学会血液委员会青年委员。
科研成果及获奖情况:
1.实用新型专利,发明名称:一种分离装置,专利号:201420394032X
2.EHA口头汇报:
1). Genetic landscapes and curative effect of CAR T-cell immunotherapy in relapse and refractory DLBCL patients.
3.ASH口头汇报:
1). Allogeneic Hematopoietic Stem Cell Transplantation with Conditioning Including Donor Humanized CAR-T Cells for Refractory/Relapsed B-Cell Non-Hodgkin Lymphoma and Multiple Myeloma
2). Auto Hematopoietic Stem Cell Transplantation Combined with Another Target Humanized CAR-T Cells for Refractory/Relapsed B-Cell Non-Hodgkin Lymphoma after Failure of Murinized CD19-CAR-T Therapy
胡凯主任出诊信息:
周一下午 13:30-16:00
周三上午 8:00-12:00





 京公网安备11010602050084号
京公网安备11010602050084号

